国家药监局发布的《关于进一步加强医疗器械注册人委托生产监督管理的公告(2024年第38号)》提到:“受托生产企业应当建立生产放行规程,明确生产放行的标准、条件,对医疗器械生产过程进行审核,对产品进行检验,确认符合标准、条件的,方可生产放行。”
那么生产放行必须把产品技术要求作为放行标准吗?是否可以根据产品特点设定生产放行标准,不把产品技术要求当成产品放行标准呢?
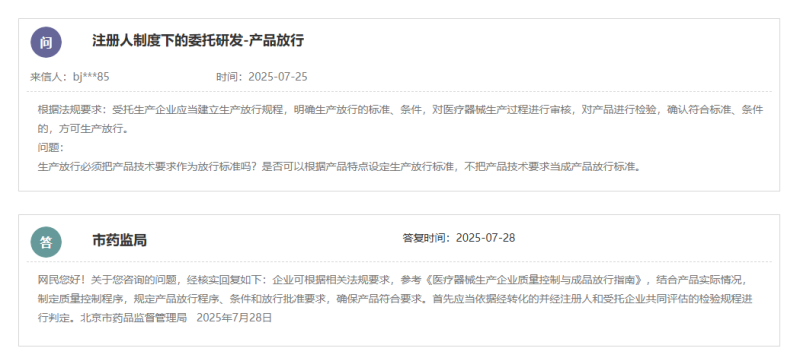
根据北京市药监局的答复,企业可根据相关法规要求,参考《医疗器械生产企业质量控制与成品放行指南》,结合产品实际情况,制定质量控制程序,规定产品放行程序、条件和放行批准要求,确保产品符合要求。首先应当依据经转化的并经注册人和受托企业共同评估的检验规程进行判定。
往期精彩推荐
医疗器械注册咨询认准金飞鹰
深圳:0755-86194173
广州:020 - 82177679
四川:028 - 68214295
湖南:0731-22881823
湖北:181-3873-5940
江苏:135-5494-7827
广西:188-2288-8311
海南:135-3810-3052
重庆:135-0283-7139


